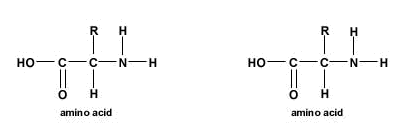Información Técnica
Información sobre Péptidos
Introducción a los Péptidos
¿Qué es un Péptido?
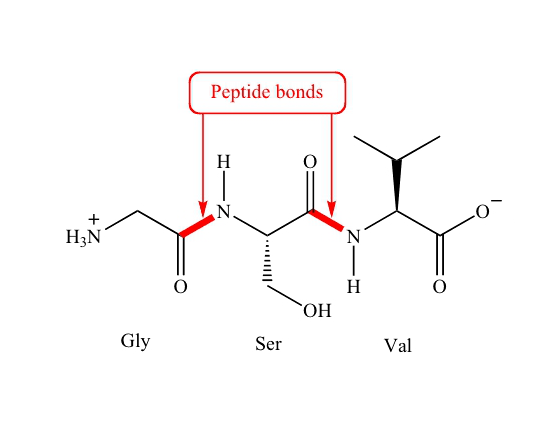
Un péptido es un compuesto químico natural que contiene dos o más aminoácidos conectados entre sí por enlaces peptídicos. Un enlace peptídico es un enlace covalente que se forma entre dos aminoácidos cuando un grupo carboxilo o extremo C de un aminoácido reacciona con el grupo amino o extremo N de otro aminoácido en una reacción de condensación (durante la reacción se libera una molécula de agua). El enlace resultante es un enlace CO-NH y forma una molécula de péptido o amida. Asimismo, los enlaces peptídicos son enlaces amida.
La palabra "péptido" proviene del griego πέσσειν, que significa "digerir". Los péptidos son una parte esencial de la naturaleza y la bioquímica, y miles de péptidos ocurren naturalmente en el cuerpo humano y en los animales. Además, se descubren y sintetizan nuevos péptidos regularmente en el laboratorio. De hecho, este descubrimiento e innovación en el estudio de los péptidos es muy prometedor para el futuro en los campos de la salud y el desarrollo farmacéutico.
¿Cómo se Forman los Péptidos?
Los péptidos se forman tanto de manera natural dentro del cuerpo como sintéticamente en el laboratorio. El cuerpo fabrica algunos péptidos de forma orgánica, como los péptidos ribosomales y no ribosomales. En el laboratorio, los procesos modernos de síntesis de péptidos pueden crear un número virtualmente ilimitado de péptidos utilizando técnicas como la síntesis en fase líquida o la síntesis en fase sólida. Si bien la síntesis en fase líquida tiene algunas ventajas, la síntesis de péptidos en fase sólida es el proceso estándar utilizado hoy en día.
El primer péptido sintético fue descubierto en 1901 por Emil Fischer en colaboración con Ernest Fourneau. La oxitocina, el primer polipéptido, fue sintetizada en 1953 por Vincent du Vigneaud.
Terminología de los Péptidos
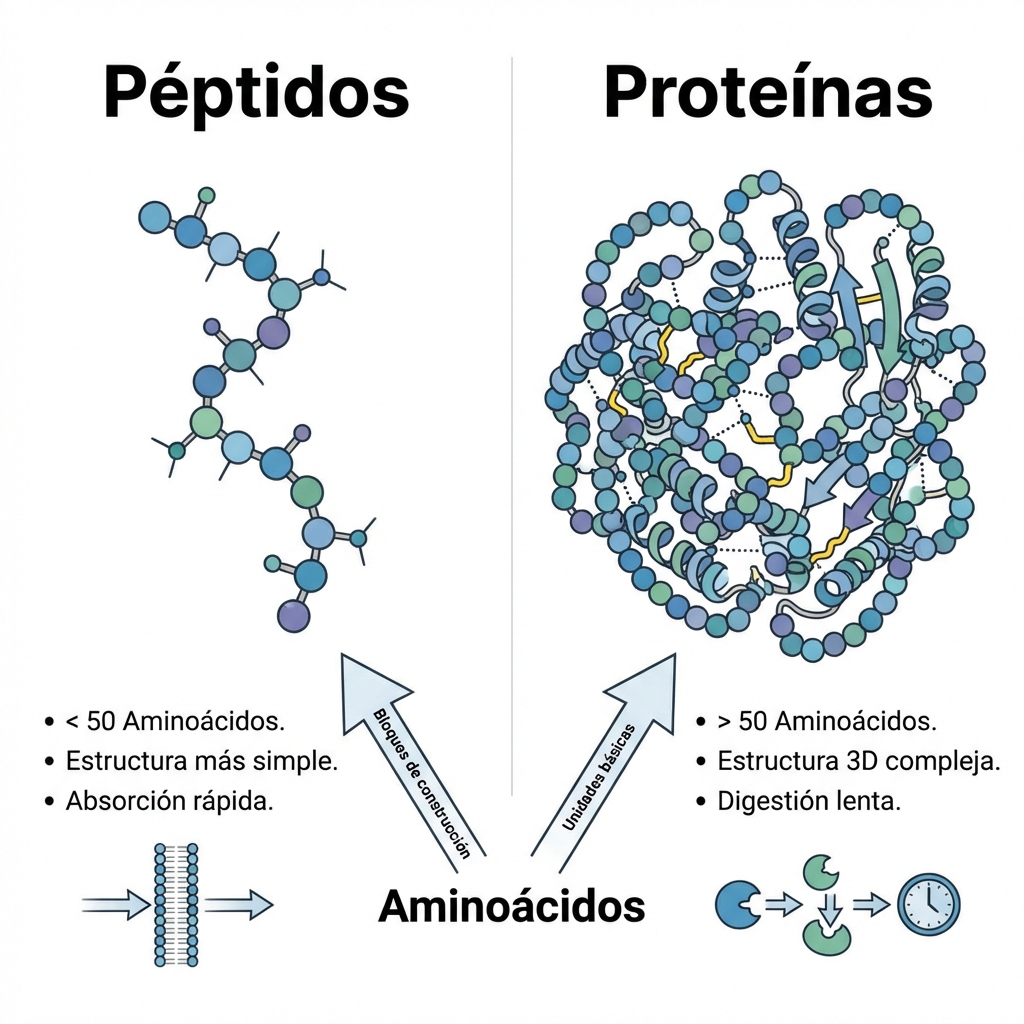
Los péptidos se clasifican generalmente según la cantidad de aminoácidos que contienen. El péptido más corto, compuesto por solo dos aminoácidos, se denomina "dipéptido". Asimismo, un péptido con 3 aminoácidos se conoce como "tripéptido". Los oligopéptidos se refieren a péptidos más cortos compuestos por un número relativamente pequeño de aminoácidos, generalmente menos de diez. Los polipéptidos, por el contrario, suelen estar compuestos por más de al menos diez aminoácidos. Los péptidos mucho más grandes (aquellos compuestos por más de 40-50 aminoácidos) generalmente se denominan proteínas.
Si bien el número de aminoácidos contenidos es un determinante principal para diferenciar entre péptidos y proteínas, a veces se hacen excepciones. Por ejemplo, ciertos péptidos más largos se han considerado proteínas (como la beta amiloide), y ciertas proteínas más pequeñas se denominan péptidos en algunos casos (como la insulina).
Clasificación de los Péptidos
Los péptidos se dividen generalmente en varias clases. Estas clases varían según cómo se producen los péptidos. Por ejemplo, los péptidos ribosomales se producen a partir de la traducción del ARNm. Los péptidos ribosomales a menudo funcionan como hormonas y moléculas de señalización en los organismos. Estos pueden incluir péptidos de taquicinina, péptidos intestinales vasoactivos, péptidos opioides, péptidos pancreáticos y péptidos de calcitonina. Los antibióticos como las microcinas son péptidos ribosomales producidos por ciertos organismos. Los péptidos ribosomales a menudo pasan por el proceso de proteólisis (la descomposición de proteínas en péptidos más pequeños o aminoácidos) para alcanzar su forma madura.
Por el contrario, los péptidos no ribosomales son producidos por enzimas específicas de péptidos, no por el ribosoma (como en los péptidos ribosomales). Los péptidos no ribosomales son frecuentemente cíclicos en lugar de lineales, aunque a menudo pueden ocurrir péptidos no ribosomales lineales. Los péptidos no ribosomales pueden desarrollar estructuras cíclicas extremadamente complejas y aparecen frecuentemente en plantas, hongos y organismos unicelulares. El glutatión, una parte clave de las defensas antioxidantes en organismos aeróbicos, es el péptido no ribosomal más común.
Los péptidos de la leche se forman a partir de las proteínas de la leche. Pueden ser producidos por descomposición enzimática mediante enzimas digestivas o por las proteinasas formadas por lactobacilos durante la fermentación de la leche. Además, las peptonas son péptidos derivados de la leche o carne animal que han sido digeridos por digestión proteolítica. Las peptonas se utilizan a menudo en el laboratorio como nutrientes para el cultivo de hongos y bacterias.
Los fragmentos de péptidos, además, se encuentran más comúnmente como productos de degradación enzimática realizada en el laboratorio sobre una muestra controlada. Sin embargo, los fragmentos de péptidos también pueden ocurrir naturalmente como resultado de la degradación por efectos naturales.
Términos Importantes sobre Péptidos
Existen algunos términos básicos relacionados con los péptidos que son clave para una comprensión general de los mismos, su síntesis y su uso en investigación y experimentación:
- Aminoácidos Los péptidos están compuestos por aminoácidos. Un aminoácido es cualquier molécula que contiene grupos funcionales tanto amina como carboxilo. Los alfa-aminoácidos son los bloques de construcción a partir de los cuales se construyen los péptidos.
- Péptidos Cíclicos Un péptido cíclico es aquel en el que la secuencia de aminoácidos forma una estructura de anillo en lugar de una cadena recta. Ejemplos de péptidos cíclicos incluyen melanotan-2 y PT-141 (Bremelanotide).
- Secuencia de Péptidos La secuencia de péptidos es simplemente el orden en el que los residuos de aminoácidos están conectados por enlaces peptídicos en el péptido.
- Enlace Peptídico Un enlace peptídico es un enlace covalente que se forma entre dos aminoácidos cuando un grupo carboxilo de un aminoácido reacciona con el grupo amino de otro aminoácido. Esta reacción es una reacción de condensación (se libera una molécula de agua).
- Mapeo de Péptidos El mapeo de péptidos es un proceso que se utiliza para validar o descubrir la secuencia de aminoácidos de péptidos o proteínas específicas. Los métodos de mapeo logran esto rompiendo el péptido o proteína con enzimas y examinando el patrón resultante de sus secuencias de aminoácidos o bases de nucleótidos.
- Miméticos de Péptidos Un mimético de péptido es una molécula que imita biológicamente ligandos activos de hormonas, citoquinas, sustratos enzimáticos, virus u otras biomoléculas. Los miméticos pueden ser péptidos naturales, péptidos modificados sintéticamente o cualquier otra molécula que realice la función mencionada.
- Huella Peptídica Una huella peptídica es un patrón cromatográfico del péptido. Se produce hidrolizando parcialmente el péptido, lo que lo rompe en fragmentos, y luego mapeando en 2D esos fragmentos resultantes.
- Biblioteca de Péptidos Una biblioteca de péptidos está compuesta por un gran número de péptidos que contienen una combinación sistemática de aminoácidos. Estas bibliotecas se utilizan a menudo en el estudio de proteínas con fines bioquímicos y farmacéuticos. La síntesis en fase sólida es la técnica más frecuente utilizada para preparar bibliotecas de péptidos.